Organisation et transformations de la matière
Une version article du chapitre pour comprendre l'essentiel rapidement, vérifier si le niveau correspond, puis basculer vers Wilo pour la pratique guidée et le suivi.
Lecture
4 chapitres
Un parcours éditorialisé et navigable.
Pratique
12 questions
Quiz et cartes mémoire à ouvrir après la lecture.
Objectif
5ème
Format rapide pour vérifier si le chapitre correspond.
Chapitre 1
La matière autour de nous
Les états physiques de la matière
La matière qui nous entoure peut exister sous trois états principaux : solide, liquide et gazeux. Ces états se distinguent par la manière dont les particules (molécules ou atomes) qui composent la matière sont organisées et interagissent.
-
État solide :
- Les particules sont très proches les unes des autres et fortement liées.
- Elles vibrent sur place mais ne peuvent pas se déplacer librement.
- Un solide possède une forme propre (définie) et un volume propre (défini).
- Exemples : un glaçon, une chaise, un caillou.
-
État liquide :
- Les particules sont proches mais moins liées que dans un solide.
- Elles peuvent glisser les unes sur les autres.
- Un liquide n'a pas de forme propre ; il prend la forme du récipient qui le contient.
- Il possède un volume propre (défini).
- Sa surface au repos est plane et horizontale.
- Exemples : l'eau, l'huile, le jus de fruit.
-
État gazeux :
- Les particules sont très éloignées les unes des autres et presque sans liens.
- Elles se déplacent dans toutes les directions, de manière désordonnée et rapide.
- Un gaz n'a ni forme propre, ni volume propre ; il occupe tout l'espace disponible.
- Il est facilement compressible et expansible.
- Exemples : la vapeur d'eau, l'air, le dioxygène.
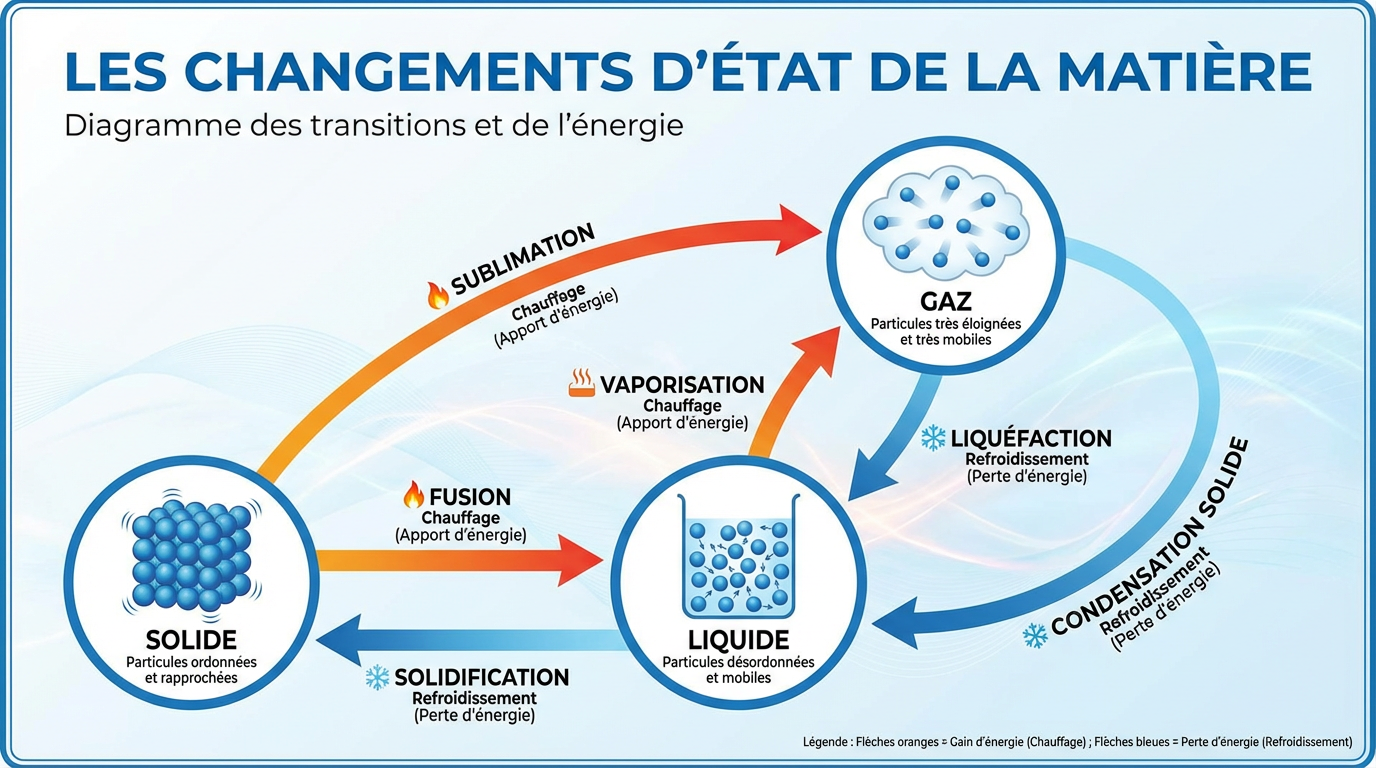
Les changements d'état
Un changement d'état est le passage d'un état physique à un autre, généralement sous l'effet d'une variation de température ou de pression. Ces transformations sont réversibles.
| Nom du changement d'état | Passage de... | À... | Explication |
|---|---|---|---|
| Fusion | Solide | Liquide | Passage d'un solide à un liquide (ex: glace qui fond). |
| Solidification | Liquide | Solide | Passage d'un liquide à un solide (ex: eau qui gèle). |
| Vaporisation | Liquide | Gaz | Passage d'un liquide à un gaz (ex: eau qui bout, évaporation). |
| Liquéfaction (ou Condensation liquide) | Gaz | Liquide | Passage d'un gaz à un liquide (ex: buée sur une vitre froide). |
| Sublimation | Solide | Gaz | Passage direct d'un solide à un gaz (ex: glace sèche). |
| Condensation solide (ou Déposition) | Gaz | Solide | Passage direct d'un gaz à un solide (ex: formation du givre). |
Pendant un changement d'état d'un corps pur, la température reste constante.
Conservation de la masse lors des changements d'état
Lors d'un changement d'état, la matière change d'apparence mais sa quantité ne change pas.
- Si l'on mesure la masse d'un système fermé (où rien ne peut entrer ou sortir) avant et après un changement d'état, on constate qu'elle reste la même.
- C'est la loi de conservation de la masse : la masse totale d'un système fermé reste constante lors d'un changement d'état.
- Exemple : Si on pèse un glaçon dans un flacon fermé, puis qu'on le laisse fondre, la masse du flacon avec l'eau liquide sera identique à la masse du flacon avec le glaçon. Les particules sont juste réorganisées.
Chapitre 2
Mélanges et corps purs
Distinction entre corps purs et mélanges
- Un corps pur est une substance composée d'un seul type de matière. Ses propriétés (température de fusion, d'ébullition) sont fixes et bien définies.
- Exemples : l'eau pure (distillée), le dioxygène, le fer.
- Un mélange est une substance composée de plusieurs corps purs différents. Ses propriétés ne sont pas fixes et dépendent de la proportion de chaque constituant.
- Exemples : l'eau salée, l'air, le jus d'orange.
Pour distinguer un corps pur d'un mélange, on peut observer sa température lors d'un changement d'état :
- Un corps pur change d'état à une température constante.
- Un mélange change d'état sur une plage de températures.
Les différents types de mélanges
Il existe deux catégories principales de mélanges :
-
Mélange homogène :
- Les différents constituants ne sont pas visibles à l'œil nu, même avec un instrument optique.
- On ne distingue qu'une seule phase.
- Exemples : l'eau salée (le sel est dissous dans l'eau), l'air (mélange de gaz), le sirop de menthe dilué.
- Le constituant majoritaire est appelé solvant (ex: l'eau). Le constituant minoritaire qui se dissout est appelé soluté (ex: le sel, le sucre).
-
Mélange hétérogène :
- Les différents constituants sont visibles à l'œil nu ou avec une loupe.
- On distingue au moins deux phases.
- Exemples : l'eau et l'huile (l'huile flotte sur l'eau), l'eau boueuse (particules de terre en suspension), le jus d'orange avec pulpe.
Techniques de séparation des mélanges
Plusieurs techniques permettent de séparer les constituants d'un mélange :
- Décantation :
- Permet de séparer un liquide d'un solide insoluble (ex: eau et sable) ou deux liquides non miscibles (ex: eau et huile).
- Les constituants se séparent sous l'effet de la gravité en fonction de leur densité. Le plus dense se dépose au fond.
- Filtration :
- Permet de séparer un liquide d'un solide insoluble (ex: eau boueuse).
- Le mélange passe à travers un filtre qui retient les particules solides. Le liquide obtenu est appelé le filtrat.
- Distillation :
- Permet de séparer les constituants d'un mélange homogène liquide (ex: eau salée).
- Le liquide est chauffé jusqu'à ébullition. La vapeur est ensuite refroidie pour la condenser et récupérer le liquide purifié (le distillat). Le solide reste dans le ballon.
- Évaporation :
- Permet de récupérer le solide dissous dans un liquide (ex: sel de l'eau salée).
- Le liquide s'évapore, laissant le solide derrière lui. Cette méthode ne permet pas de récupérer le liquide.
La solubilité
La solubilité est la capacité d'une substance (le soluté) à se dissoudre dans une autre substance (le solvant).
- Elle s'exprime souvent en grammes de soluté par litre de solvant (g/L) ou par 100 mL (g/100 mL).
- Une solution est dite saturée lorsque le solvant ne peut plus dissoudre de soluté. Tout ajout de soluté restera non dissous.
- Facteurs influençant la solubilité :
- La température : généralement, la solubilité des solides augmente avec la température (ex: plus de sucre dans l'eau chaude).
- L'agitation : elle accélère la dissolution mais n'augmente pas la quantité maximale de soluté qui peut être dissoute.
- La nature du soluté et du solvant.
Chapitre 3
L'air qui nous entoure
Composition de l'air
L'air est un mélange gazeux homogène indispensable à la vie sur Terre.
Sa composition est quasiment constante :
- Environ 78 % de diazote ()
- Environ 21 % de dioxygène ()
- Environ 1 % d'autres gaz, dont l'argon, le dioxyde de carbone (), la vapeur d'eau, etc.
Le dioxygène est le gaz le plus important pour la respiration et la combustion.
Propriétés de l'air
L'air, bien qu'invisible, possède des propriétés physiques mesurables :
- Masse de l'air : L'air a une masse. Un litre d'air à 0°C et pression atmosphérique normale pèse environ 1,29 gramme.
- Pression atmosphérique : L'air exerce une pression sur toutes les surfaces. C'est le poids de la colonne d'air au-dessus de nous. Elle est mesurée avec un baromètre.
- Compressibilité : Le volume de l'air peut être réduit en augmentant la pression. Les particules se rapprochent.
- Expansibilité : L'air peut occuper un volume plus grand si la pression diminue. Les particules s'éloignent.
Le dioxygène, un gaz indispensable
Le dioxygène est un gaz incolore, inodore et insipide, essentiel à la vie.
- Combustion : Le dioxygène est le comburant indispensable à la plupart des combustions. Sans lui, un feu ne peut pas brûler.
- Respiration : Tous les êtres vivants (animaux et plantes) utilisent le dioxygène pour respirer, c'est-à-dire pour produire l'énergie nécessaire à leurs fonctions vitales.
- Test du dioxygène : On peut mettre en évidence le dioxygène avec une bûchette incandescente (une allumette que l'on a soufflée et qui a encore une petite braise). En présence de dioxygène, la bûchette se rallume.
Chapitre 4
Les transformations chimiques
Distinction entre transformation physique et chimique
-
Une transformation physique :
- Change l'état ou l'apparence de la matière, mais pas sa nature.
- Les substances de départ (les corps purs) sont les mêmes que les substances d'arrivée.
- Exemples : la fusion de la glace, la dissolution du sucre dans l'eau, casser un verre.
-
Une transformation chimique (ou réaction chimique) :
- Modifie la nature des substances.
- Des substances de départ appelées réactifs disparaissent et de nouvelles substances, les produits, apparaissent.
- Exemples : la combustion d'une bougie, la rouille du fer, la digestion des aliments.
- On observe souvent des signes d'une transformation chimique : changement de couleur, dégagement de gaz, production de chaleur ou de lumière, formation d'un précipité.
Exemples de transformations chimiques courantes
- Combustion : Réaction rapide d'une substance (le combustible) avec le dioxygène (le comburant), produisant de la chaleur, de la lumière et de nouvelles substances (produits de combustion, ex: dioxyde de carbone et eau).
- Exemple : La combustion du bois, du gaz, d'une bougie.
- Oxydation : Réaction d'une substance avec le dioxygène, généralement plus lente que la combustion.
- Exemple : La formation de la rouille sur le fer (oxydation du fer).
- Fermentation : Transformation de substances organiques par des micro-organismes (levures, bactéries) en l'absence de dioxygène.
- Exemple : La transformation du jus de raisin en vin, du lait en yaourt.
- Réaction acide-base : Réaction entre un acide et une base.
- Exemple : Le vinaigre (acide) et le bicarbonate de soude (base) produisent un dégagement gazeux.
Conservation de la masse lors d'une transformation chimique
La loi de Lavoisier, également appelée loi de conservation de la masse, stipule que :
- Au cours d'une transformation chimique, la masse totale des réactifs consommés est égale à la masse totale des produits formés.
- En d'autres termes, rien ne se perd, rien ne se crée, tout se transforme.
- Pour que cette loi soit vérifiée, la réaction doit se dérouler dans un système fermé (où aucune matière ne peut entrer ou sortir).
- Exemple : Si on fait brûler une bougie dans un système fermé (ex: sous une cloche), la masse totale du système (bougie, dioxygène, produits de combustion) reste constante.
Après la lecture
Passe à la pratique avec deux blocs bien visibles
Une fois le cours lu, ouvre soit le quiz pour vérifier la compréhension, soit les flashcards pour mémoriser les idées importantes. Les deux s'ouvrent dans une fenêtre dédiée.
Suite naturelle
Tu veux aller plus loin que l'article ?
Retrouve le même chapitre dans Wilo avec la suite des questions, la répétition espacée, les corrigés complets et une progression suivie dans le temps.