Organisation et transformations de la matière
Une version article du chapitre pour comprendre l'essentiel rapidement, vérifier si le niveau correspond, puis basculer vers Wilo pour la pratique guidée et le suivi.
Lecture
5 chapitres
Un parcours éditorialisé et navigable.
Pratique
12 questions
Quiz et cartes mémoire à ouvrir après la lecture.
Objectif
4ème
Format rapide pour vérifier si le chapitre correspond.
Chapitre 1
I. Les états de la matière et leurs changements
1. Les trois états physiques de la matière
La matière qui nous entoure peut exister sous trois états principaux, facilement observables :
- Solide : Il a une forme propre et un volume propre. Il est difficile à déformer.
- Exemple : un glaçon, une pierre.
- Liquide : Il n'a pas de forme propre, il prend la forme du récipient qui le contient. Il a un volume propre. Sa surface est plane et horizontale au repos.
- Exemple : l'eau liquide, l'huile.
- Gazeux : Il n'a ni forme propre, ni volume propre. Il occupe tout le volume disponible du récipient qui le contient. Il est compressible et expansible.
- Exemple : la vapeur d'eau, l'air.
2. Modèle particulaire des états de la matière
Pour comprendre le comportement de la matière, on utilise le modèle particulaire. Ce modèle imagine que toute matière est constituée de minuscules éléments appelés particules (qui peuvent être des atomes ou des molécules).
- État solide : Les particules sont très proches les unes des autres, rangées de manière ordonnée et faiblement agitées (elles vibrent sur place). Les forces d'interaction entre elles sont très fortes.
- État liquide : Les particules sont proches, mais désordonnées. Elles peuvent glisser les unes sur les autres. Elles sont moyennement agitées. Les forces d'interaction sont moins fortes que dans les solides.
- État gazeux : Les particules sont très éloignées les unes des autres et très agitées. Elles se déplacent de manière désordonnée et rapide dans tout le volume disponible. Les forces d'interaction entre elles sont quasi nulles.
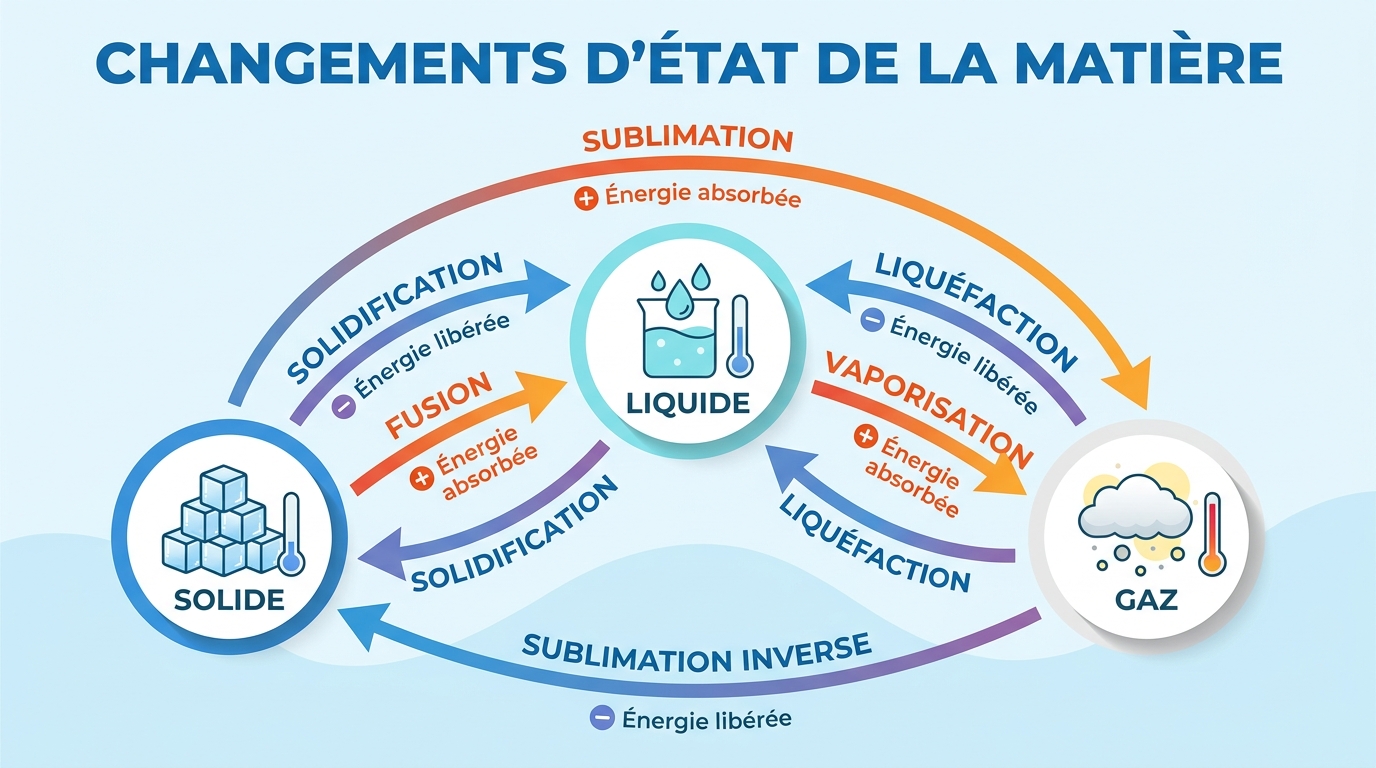
3. Changements d'état physique
Un changement d'état est le passage d'un état physique à un autre, sans modification de la nature de la substance.
| Changement d'état | Passage de | Nom spécifique |
|---|---|---|
| Fusion | Solide vers Liquide | Fusion |
| Solidification | Liquide vers Solide | Solidification |
| Vaporisation | Liquide vers Gazeux | Vaporisation (ébullition ou évaporation) |
| Liquéfaction | Gazeux vers Liquide | Liquéfaction ou Condensation liquide |
| Sublimation | Solide vers Gazeux | Sublimation |
| Condensation | Gazeux vers Solide | Condensation solide ou Déposition |
Pour un corps pur, les changements d'état se produisent à une température constante et caractéristique (par exemple, 0°C pour la fusion/solidification de l'eau pure). Lors d'un changement d'état, la masse est conservée. Seul le volume peut changer.
4. Énergie et changements d'état
Les changements d'état nécessitent un apport ou une libération d'énergie, souvent sous forme d'énergie thermique (chaleur).
- Changements endothermiques (qui absorbent de l'énergie) : Fusion, vaporisation, sublimation. Il faut apporter de la chaleur.
- Exemple : un glaçon fond en absorbant la chaleur ambiante.
- Changements exothermiques (qui libèrent de l'énergie) : Solidification, liquéfaction, condensation. La substance libère de la chaleur.
- Exemple : l'eau gèle en libérant de la chaleur.
Chapitre 2
II. L'air qui nous entoure
1. Composition de l'air
L'air est un mélange de gaz transparent et inodore. Ce n'est pas un corps pur !
Sa composition principale est :
- Environ 78 % de diazote ()
- Environ 21 % de dioxygène ()
- Environ 1 % d'autres gaz, dont l'argon (), le dioxyde de carbone (), et la vapeur d'eau.
2. Propriétés physiques de l'air
- Masse de l'air : L'air a une masse. Un litre d'air à 0°C et pression normale pèse environ 1,29 gramme.
- Volume de l'air : L'air est un gaz, il occupe tout le volume disponible.
- Pression atmosphérique : L'air exerce une pression sur toutes les surfaces en contact. Cette pression est due au poids de la colonne d'air au-dessus de nous. La pression atmosphérique normale est d'environ 1013 hPa (hectopascals) au niveau de la mer.
3. Le rôle du dioxygène
Le dioxygène () est un gaz essentiel à la vie et à de nombreuses transformations.
- Il est indispensable à la respiration des êtres vivants.
- C'est un réactif essentiel dans les phénomènes de combustion (brûler quelque chose).
Chapitre 3
III. Les mélanges et les corps purs
1. Corps purs et mélanges
- Un corps pur est une substance constituée d'un seul type de matière (par exemple, l'eau pure, le dioxygène). Il a des propriétés physiques (température de fusion, d'ébullition) caractéristiques et constantes.
- Un mélange est une substance constituée de plusieurs corps purs.
- Exemples : l'eau salée, l'air, le jus d'orange.
2. Types de mélanges
Il existe deux catégories de mélanges :
- Mélange homogène : On ne peut pas distinguer les différents constituants à l'œil nu, même avec une loupe. Le mélange a un aspect uniforme.
- Exemples : l'eau salée (le sel est dissous), l'air, le sirop de menthe. On parle souvent de solution quand un solide est dissous dans un liquide.
- Mélange hétérogène : On peut distinguer à l'œil nu au moins deux constituants. Le mélange n'a pas un aspect uniforme.
- Exemples : l'eau et l'huile, l'eau boueuse (particules en suspension), le jus d'orange avec pulpe.
3. Techniques de séparation des mélanges
Plusieurs techniques permettent de séparer les constituants d'un mélange :
- Décantation : Pour séparer un liquide et un solide insoluble (ou deux liquides non miscibles) par simple repos. Le constituant le plus dense se dépose au fond.
- Filtration : Pour séparer un liquide d'un solide insoluble en utilisant un filtre. Le solide (résidu) est retenu par le filtre, le liquide (filtrat) passe à travers.
- Distillation : Pour séparer les constituants d'un mélange homogène liquide, en profitant de leurs différentes températures d'ébullition. Le liquide qui bout en premier est récupéré après condensation.
- Chromatographie : Technique plus avancée pour séparer les constituants d'un mélange en fonction de leur affinité pour une phase stationnaire et une phase mobile.
4. Solubilité et concentration
Lorsqu'on dissout un solide dans un liquide :
- Le solvant est le liquide (ex: l'eau).
- Le soluté est le solide que l'on dissout (ex: le sel).
- Le mélange obtenu est une solution.
La solubilité d'une substance est la masse maximale de soluté que l'on peut dissoudre dans un volume donné de solvant à une température donnée.
- Si on ajoute trop de soluté, la solution devient une solution saturée : le soluté en excès ne se dissout plus et reste visible au fond.
Chapitre 4
IV. Les transformations chimiques
1. Distinction entre transformation physique et chimique
Il est crucial de distinguer :
- Une transformation physique : La nature des substances ne change pas. Seul l'état ou l'aspect change. Les molécules restent les mêmes.
- Exemples : la fusion d'un glaçon (l'eau reste de l'eau), la dissolution du sel dans l'eau.
- Une transformation chimique : De nouvelles substances (les produits) sont formées à partir des substances de départ (les réactifs). Les molécules initiales sont rompues et de nouvelles molécules sont formées.
- Exemples : la combustion d'une bougie, la formation de rouille sur le fer, la cuisson d'un gâteau. La nature des substances est modifiée en profondeur.
2. Les réactifs et les produits
Dans une transformation chimique :
- Les réactifs sont les substances qui disparaissent. Ce sont les ingrédients de départ.
- Les produits sont les nouvelles substances qui apparaissent. Ce sont les résultats de la transformation.
On représente une transformation chimique par une équation de réaction (qualitative au niveau 4ème) : Réactifs Produits Exemple : Pour la combustion du carbone : Carbone + Dioxygène Dioxyde de carbone
3. La conservation de la masse
La loi de Lavoisier (ou loi de conservation de la masse) est fondamentale en chimie : Lors d'une transformation chimique, la masse totale des réactifs est égale à la masse totale des produits. "Rien ne se perd, rien ne se crée, tout se transforme." Cela signifie que la matière est réorganisée, mais pas créée ni détruite.
4. Exemples de réactions chimiques courantes
- Combustion du carbone : Carbone (solide) + Dioxygène (gaz) Dioxyde de carbone (gaz).
- Combustion du méthane (gaz naturel) : Méthane + Dioxygène Dioxyde de carbone + Eau.
- Oxydation du fer (rouille) : Fer + Dioxygène Oxyde de fer (rouille). C'est une combustion lente.
- Réaction acide-base (introduction) : Transformation où un acide réagit avec une base. Exemple : Vinaigre (acide) + Bicarbonate de soude (base) Gaz carbonique + Eau + Sel.
Chapitre 5
V. Atomes et molécules
1. Le modèle de l'atome
- L'atome est le constituant fondamental et indivisible de la matière (à notre échelle). Tout est fait d'atomes.
- On représente souvent les atomes comme de minuscules sphères de différentes couleurs et tailles pour les distinguer.
- Il existe différents types d'atomes, chacun ayant un nom et un symbole chimique :
- Carbone () : souvent représenté en noir.
- Oxygène () : souvent représenté en rouge.
- Hydrogène () : souvent représenté en blanc.
- Azote () : souvent représenté en bleu.
2. Les molécules
- Une molécule est un assemblage d'au moins deux atomes liés entre eux. Ces atomes peuvent être identiques ou différents.
- La formule chimique d'une molécule indique la nature et le nombre de chaque type d'atome qui la compose.
- : une molécule de dioxygène contient deux atomes d'oxygène.
- : une molécule d'eau contient deux atomes d'hydrogène et un atome d'oxygène.
- : une molécule de dioxyde de carbone contient un atome de carbone et deux atomes d'oxygène.
- Les modèles moléculaires (boules et bâtonnets) permettent de visualiser la géométrie des molécules.
3. Interprétation des transformations chimiques au niveau atomique
Au cours d'une transformation chimique :
- Les molécules des réactifs se cassent (les liaisons entre atomes se rompent).
- Les atomes se réarrangent pour former de nouvelles liaisons.
- De nouvelles molécules (les produits) sont créées.
- Les atomes eux-mêmes ne sont ni créés ni détruits, ils sont simplement réorganisés. C'est pourquoi la masse se conserve !
- Si j'ai 10 atomes de carbone au début, j'aurai toujours 10 atomes de carbone à la fin, mais ils seront peut-être liés à d'autres atomes pour former de nouvelles molécules.
Après la lecture
Passe à la pratique avec deux blocs bien visibles
Une fois le cours lu, ouvre soit le quiz pour vérifier la compréhension, soit les flashcards pour mémoriser les idées importantes. Les deux s'ouvrent dans une fenêtre dédiée.
Suite naturelle
Tu veux aller plus loin que l'article ?
Retrouve le même chapitre dans Wilo avec la suite des questions, la répétition espacée, les corrigés complets et une progression suivie dans le temps.